Naukowcy od dawna wiedzą, że mleko kobiece dostarcza noworodkom istotnych składników odżywczych, a przeciwciała, które matka nabywa w wyniku przechorowania lub szczepienia mogą być przekazywane dziecku wraz z pokarmem naturalnym. Najnowsze badania przedkliniczne wskazują, że specyficzny zestaw przeciwciał indukowanych naturalnie przez bakterie jelitowe przechodzi do organizmu niemowlęcia spożywającego mleko matki i wspomagają jego odporność przeciwko infekcjom przebiegającym z biegunką.
W artykule opublikowanym w czasopiśmie Sciene Immunology zespół naukowy z Weill Cornell Medicine w USA przedstawił wnioski ze swojej pracy; badacze skupili się na jednej z klas przeciwciał, immunoglobulinie IgG, wspomagającej organizm w walce i eliminacji zakażeń wirusowych i bakteryjnych. Do tej pory niewiele wiedzieliśmy na temat tego w jaki sposób przeciwciała IgG wytwarzane naturalnie w wyniku interakcji bakterii zasiedlających jelita z układem immunologicznym gospodarza, wpływają na odporność związaną ze śluzówką jelit u niemowląt. Opierając się na modelu mysim badacze chcieli sprawdzić w jaki sposób ten typ immunoglobulin transportowany jest z krwioobiegu matki do gruczołów mlecznych i dalej do mleka, a także jak chroni mysie noworodki przed infekcją Citrobacter rodentium (odpowiednik bakterii Escherichia coli, pałeczka okrężnicy), która stanowi potencjalny czynnik etiologiczny poważnego zakażenia przewodu pokarmowego.
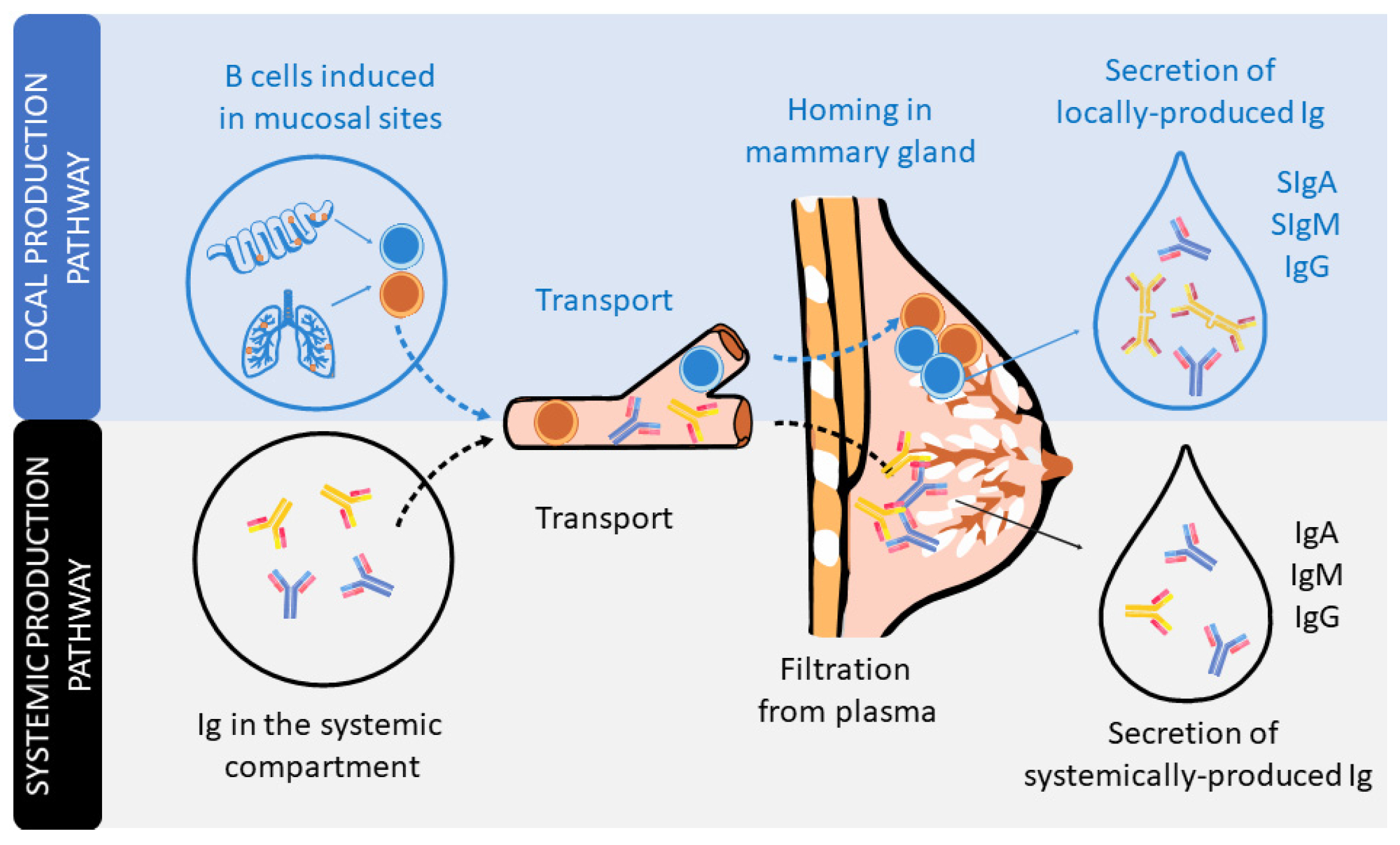
Wydzielanie przeciwciał w mleku ludzkim. Rysunek przedstawia szlak odpowiedzialny za miejscową produkcję immunoglobulin obejmujący migrację limfocytów B do gruczołu sutkowego i proces wydzielniczy oraz szlak ogólnoustrojowy obejmujący filtrację monomerycznych cząsteczek immunoglobulin z osocza.
„Odkryliśmy, że przeciwciała IgG chronią maluchy przed rozwojem choroby, a także że jesteśmy w stanie wzmocnić ten ochrony efekt”, mówi Melody Zeng, autorka badania, która w swoich projektach koncentruje się na badaniu roli mikrobiomu jelitowego i matczyno-płodowej/noworodkowej interakcji reakcji immunologicznej w rozwoju chorób zapalnych, z uwzględnieniem takich czynników jak poród przedwczesny, martwicze zapalenie jelit, alergie pokarmowe, astma i nowotwory.
Podobnie jak w przypadku przeciwciał skierowanych przeciwko wirusowi SARS-CoV-2 wykrywanych w mleku kobiet uprzednio szczepionych preparatem mRNA, naukowcy starali się zapewnić dodatkową odporność przed infekcją jelitową u niemowląt wzbudzając najpierw ochronę opartą na przeciwciałach IgG u ich matek. Do opracowania szczepionki wykorzystano składnik występujący u bakterii jelitowych, a następnie podano preparat samicom myszy jeszcze przed zajściem w ciążę.
„Ten sam mechanizm, zgodnie z którym szczepienie podwyższa poziom przeciwciał IgG u myszy i przenosi odporność na jej potomstwo, może odpowiadać za efekt ochronny także u ludzkich niemowląt”, twierdzi dr Zeng. „Strategia ta może być szczególnie korzystna w przypadku wcześniaków, ze względu na większe ryzyko rozwoju chorób biegunkowych u tak małych dzieci.”
Infekcje związane z biegunką stanowią poważne zagrożenie dla niemowląt i dzieci we wczesnym okresie życia. Według szacunków WHO biegunki są drugą najczęstszą przyczyną zgonów wśród dzieci poniżej 5 roku życia.
W swoich doświadczeniach dr Katherine Sanidad i dr Mohammed Amir współpracującyc z dr Zeng, po raz pierwszy wykazali, że przeciwciała IgG (które mysie niemowlęta nabyły wraz z mlekiem matki) zapobiegały przyczepianiu się bakterii chorobotwórczych do śluzówki jelit, co jest charakterystyczne na wczesnym etapie zakażenia.
Badaczy ciekawiło również w jaki sposób przeciwciała IgG oddziałują z innym zestawem drobnoustrojów – pożytecznymi bakteriami bytującymi naturalnie w jelitach. Pracując ze zwierzętami chcieli dowiedzieć się jak można wspierać rozwój zdrowego mikrobiomu u ludzi. Okazało się, że bakterie komensalne wspierają dojrzewanie i funkcje układu immunologicznego, między innymi poprzez „szkolenie” w rozpoznaniu swoich chorobotwórczych pobratymców.
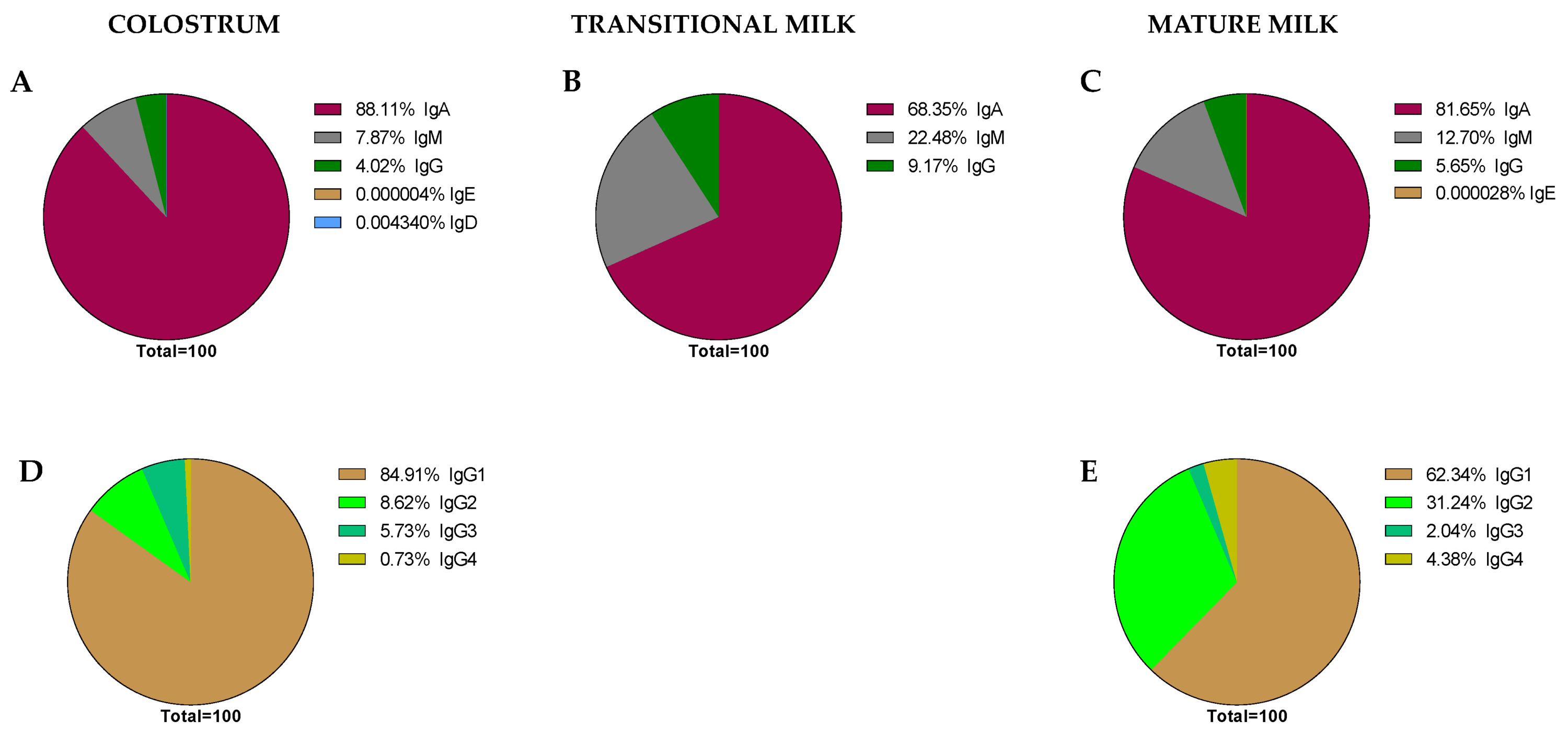
Proporcje stężęń immunoglobulin na każdym etapie laktacji: siara (A), mleko przejściowe (B), mleko dojrzałe (C). Dla podklasy IgG wartości wyrażono w siarze (D) i mleku dojrzałym (E) ze względu na brak aktualnych danych odnośnie mleka przejściowego.
Praca dr Zeng ujawniła również długofalowy efekt działania przeciwciał IgG. Mysie oseski, które nigdy nie otrzymały matczynych IgG rozwinęły w jelitach nieprawidłową mikrobiotę, co z kolei pociągnęło za sobą zmiany w działaniu układu odpornościowego – w szczególności podwyższył się poziom limfocytów T wytwarzających interleukinę IL-17 (cytokina prozapalna). Te same myszy w dorosłości wykazywały większą podatność na wystąpienie patologicznych stanów zapalnych związanych z nieswoistym zapaleniem jelit.
„Nasze odkrycie podkreśla korzyści płynące z karmienia mlekiem kobiecym dla dojrzewania układu immunologicznego, zarówno w wymiarze krótko jak i długofalowym,” mówi dr Zeng.
- Sanidad KZ, Amir M, Ananthanarayanan A, et al. Maternal gut microbiome–induced IgG regulates neonatal gut microbiome and immunity. Sci Immunol. 2022;7(72):eabh3816. doi:10.1126/sciimmunol.abh3816
- Weill Cornell Medicine. „IgG antibodies in breast milk help shape infants’ gut bacteria and immunity.” 10 June 2022.
- Rio-Aige, Karla et al. “The Breast Milk Immunoglobulinome.” Nutrients vol. 13,6 1810. 26 May. 2021, doi:10.3390/nu13061810
Podobne artykuły:
W czasie ciąży, subtelna zmiana molekularna pozwala immunoglobulinom G (IgG), które stanowią najpowszechniejszy typ przeciwciał występujący w organizmie, na pełnienie skuteczniejszej roli ochronnej przed zakażeniami. Zdaniem naukowców, ten naturalny proces można odtworzyć, dzięki czemu możliwe będzie zwiększenie skuteczności szczepionek i innych terapii opartych na działaniu przeciwciał.

Do tej pory rozwój układu odpornościowego u płodu stanowił pewną zagadkę, jednak niedawno opublikowane wyniki sugerują, że komórki dendrytyczne pojawiają się w organizmie wcześnie, już w drugim trymestrze ciąży, a jednym z ich zadań jest hamowanie reakcji immunologicznej na komórki matczyne.
Odpowiedź immunologiczna zależy od płci
Układ odpornościowy mężczyzny i kobiety reaguje odmiennie na zakażenie. Badania przedstawione w ubiegłym tygodniu na spotkaniu mikrobiologów w Bostonie sugerują, że różnice te mogą wpłynąć na opracowanie np. programów szczepień czy bardziej ukierunkowanych terapii.

Wiedza na temat ochronnych właściwości mleka kobiecego jest znana już od dawna; jednym z mechanizmów odpowiedzialnych za taki efekt jest transfer przeciwciał, wpływający na tzw. “odporność bierną”. Zespół naukowców z University of California z Riverside udowodnił, że oprócz tego, mleko ma również duży wpływ na tworzenie układu odpornościowego dziecka przez proces, który nazwano “matczyną edukacją odporności”.